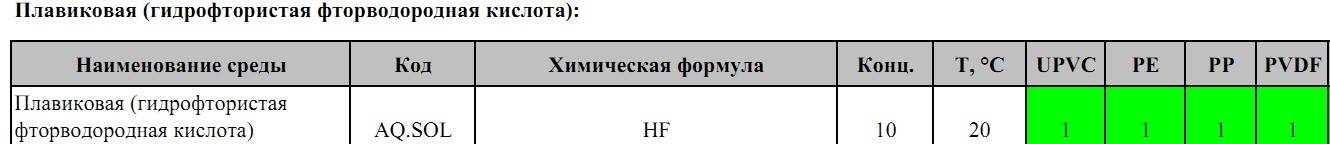
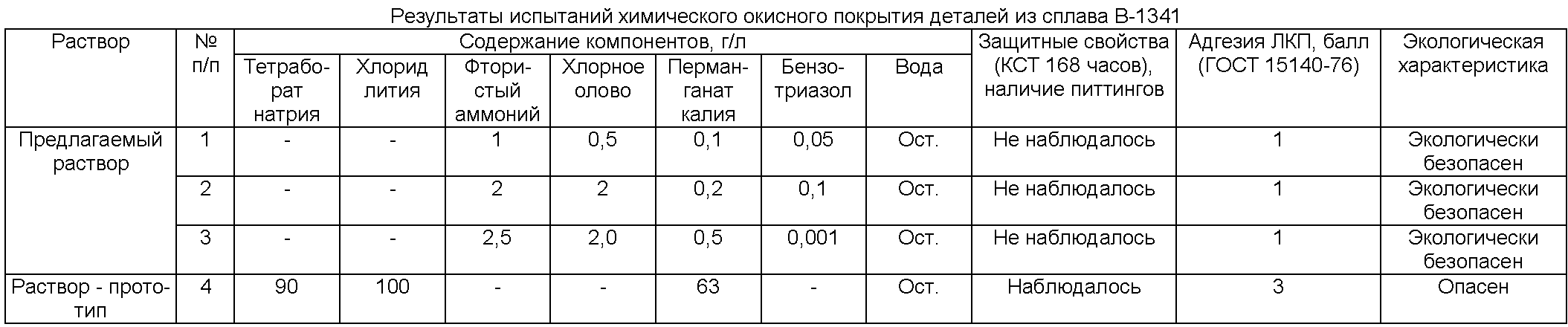
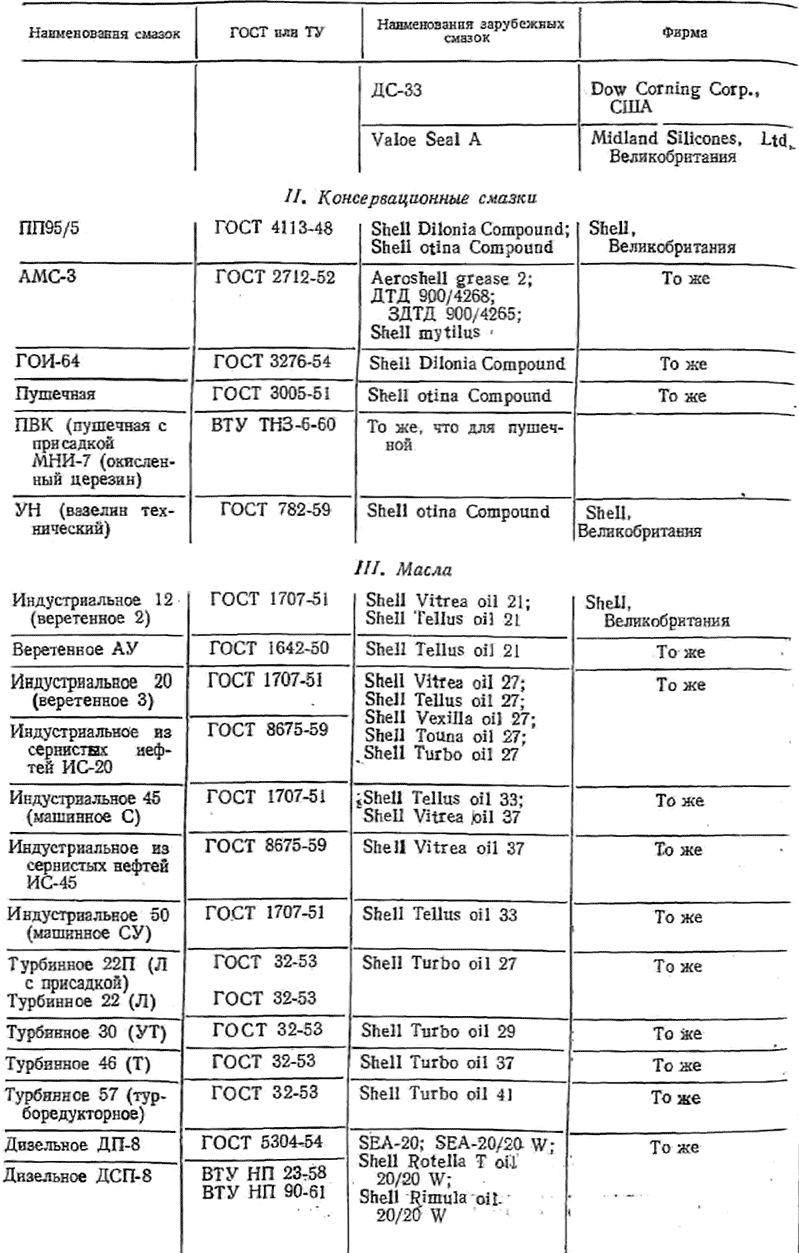
Уход за нержавеющей сталью
Было бы наивным предполагать, что изделия из нержавеющих сплавов сами по себе будут сохранять свой элегантный и нарядный внешний вид в ходе длительной эксплуатации. Для сохранения рабочих качеств и внешнего вида нержавейки за ней потребуется соответствующий периодический уход. В обычных условиях, когда используется химически нейтральная неагрессивная среда при обычных температурах, может быть достаточным регулярное промывание изделий теплой водой с мыльным раствором. Не рекомендуется использовать моющие и чистящие средства на основе аммиака или абразивных порошков. При появлении первых признаков точечной коррозии, таких, как пятна и точки, их следует удалить жесткой щеткой или плотной губкой. Если процесс продолжает развиваться, потребуется использование более серьезных восстанавливающих средств. Такие составы, ка Cilitили Цинкарь неплохо справляются на начальных этапах. Подойдет также т 8-% раствор лимонной кислоты. После использования восстанавливающих средства обработанные места следует промыть большим количеством воды.
Защита ингибиторами коррозии

Ингибитор коррозии металлов получил широкое распространение в современном мире. Группа веществ блокирует взаимодействие металла с воздухом или агрессивными средами. Данное качество ингибиторов обладает большим практическим значением. Оно позволяет сохранить целостность металла на длительное время. Данный процесс относится к разряду электрохимических.
Ингибиторы действую на металлы следующим образом: вещество попадает на металлический материал и впитывается в него. После этого металл приобретает положительный потенциал, который делает процесс образования ржавчины намного более медленным.
В современном мире применительно к металлам ингибиторами стали называть вещества, которые образуют на их поверхности тонкую, но прочную пленку, которая предотвращает попадание на поверхность металлического материала воздуха или влаги.
В настоящее время существует огромное множество веществ, которые можно использовать в качестве ингибиторов для блокирования процесса образования коррозии на поверхности металлических предметов или объектов. Самым большим количеством качеств ингибиторов обладают такие типы веществ как:
- Амины
- Азотсодержащие гетероциклические соединения
- Мочевина
- Тиолы
- Альдегиды
- Сульфиды
Способы защиты от питтинга
Существует ряд современных методов предотвращения коррозии, и многие из них применяются уже на стадии производства авто. Тем не менее, старые машины вследствие долгой эксплуатации, постоянного контакта с агрессивными реагентами подвержены ржавлению. Питтинг нередко возникает на различных деталях автомобиля: подшипниках, зубьях шестерен, а точки ржавчины на кузове и вовсе считаются распространенным явлением.
Точечная коррозия зачастую выявляется и на бытовых предметах, в том числе из нержавеющей стали. Для защиты металла можно применять механические и химические методики, некоторые из них подходят для самостоятельного использования.
Механический способ
Данный метод включает советы по удалению уже имеющейся ржавчины при помощи шлифования, лазерной обработки, а также механическое нанесение барьерных покрытий (в том числе лакокрасочных). Выбор вида покрытия зависит от типа металла и условий его эксплуатации. Обычно используется техника цинкования или никелирования, но в промышленных условиях также практикуется хромирование, покрытие медью, серебром, алюминием, оловом, кадмием. Созданная пленка изолирует металл от окружающей среды и не дает ему контактировать с кислотами, кислородом, хлором, чем продлевает срок службы.

В продаже есть наборы для самостоятельного проведения цинкования металла. Вначале производят очистку детали от уже имеющейся ржавчины путем обработки преобразователями. Через полчаса средства смывают, изделие чистят, полируют, наносят слой специального раствора и подключают электрод с цинковым наконечником. По истечении определенного времени на поверхности металла будет создана тонкая цинковая пленка, которая не позволит ржавчине и дальше разрушать материал.
Химический способ
Основным химическим методом избавления от коррозии является ликвидация замкнутой системы растворами щелочей, сульфатов, хроматов. Принцип действия заключается в уменьшении кислотности и сдвиге реакции в сторону щелочной, в которой процессы коррозии останавливаются
Важно только контролировать выделение водорода, поскольку этот элемент сам по себе увеличивает риск появления питтингов

К сожалению, в быту полностью устранить опасность развития точечной коррозии невозможно. Есть шанс лишь ослабить влияние факторов риска. Лучше сразу правильно эксплуатировать изделие, не допускать повышения кислотности среды, чем можно продлить срок его службы на несколько лет.
Питтинговая коррозия
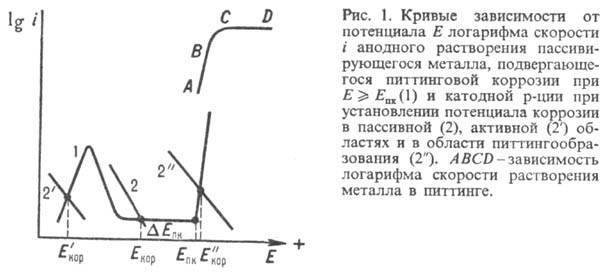
Питтинговая коррозия ( ПК) является одним из наиболее опасных видов локальной коррозии. Ей подвержены многие пассивирующиеся металлы и сплавы.
Питтинговая коррозия развивается в растворах, содержащих одновременно анионы-активаторы и окислители, такие как Fe3, Си2 1, Н2С2, растворенные газы – О2 и СО2 – Металл подвергается питтинговой коррозии в том случае, если окислительно-восстановительный потенциал раствора положительнее потенциала питтингообразования.
Питтинговая коррозия представляет один из опасных видов коррозионного разрушения, характерного для пассивного состояния металлов и сплавов. В этих случаях коррозии отдельные ограниченные участки металла растворяются со значительной скоростью, причем вся остальная поверхность может оставаться в пассивном состоянии, почти не затронутой коррозией. Это приводит к образованию глубоких поражений – точечных язв или питтингов.
Питтинговая коррозия наблюдается также в растворах, содержащих ионы С1ОГ на различных металлах: железе, цирконии, алюминии. Особенностью питтинговой коррозии в растворах с С1ОГ является то, что она возникает при значительно более положительных потенциалах, чем в растворах с галоидными ионами и, следовательно, значительно реже встречается на практике.
Питтинговая коррозия зависит от свойств морской воды.
Питтинговая коррозия никеля и никелевых сплавов возникает при нарушении пассивности в отдельных точках поверхности, экспонируемой в агрессивной среде. В таких точках происходит анодное растворение, в то время как большая часть поверхности остается пассивной. Питтинговая коррозия на никеле развивается преимущественно вблизи структурных дефектов, например границ зерен, а также на повреждениях поверхности, таких как царапины. Уменьшить вероятность питтингообразования на повреждениях поверхности можно с помощью электрополирования, но к структурным дефектам это относится в меньшей степени. На практике Питтинговая коррозия никеля и никелевых сплавов возникает в коррозионно-активных средах, содержащих хлориды или другие агрессивные ионы, а кроме того, она более вероятна в кислых, чем в щелочных или нейтральных растворах.
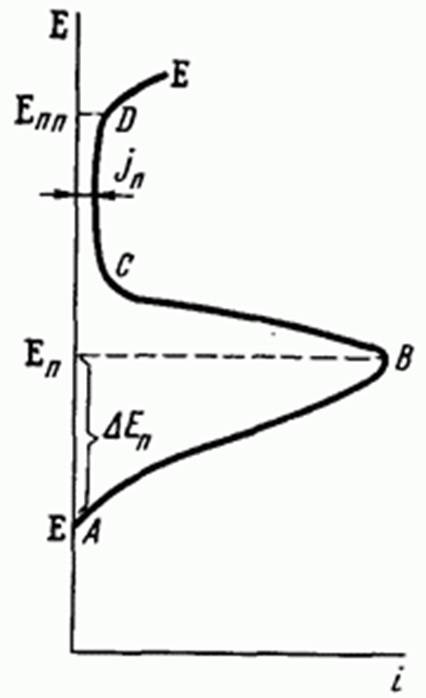
| Анодная поляризационная кривая алюминия в 3 % – ном растворе NaCl, . д – стандартный равновесный потенциал. Еп, t – потенциал и плотность тока пассивации соответственно.. пп, inn – потенциал и плотность тока полной пассивации соответственно. Епп – потенциал пробоя ( ]. |
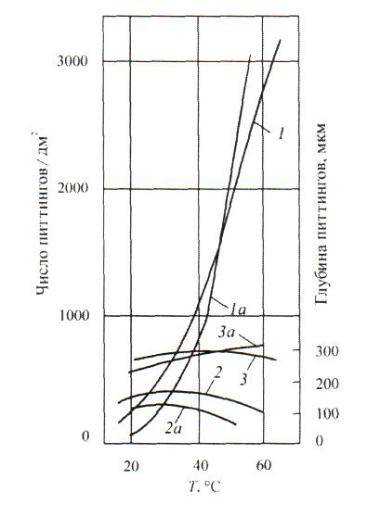
Обычно питтинговая коррозия характеризуется числом питтингов на 1 см2 при визуальном определении. При инструментальном исследовании с помощью оптической и особенно электронной микроскопии существенно увеличивается плотность видимого питтинга, выявляются структурные неоднородности мест образования и морфологические особенности питтинга.
Питтинговая коррозия никеля и никелевых сплавов, как и других металлов и сплавов, возникает при нарушении пассивности в отдельных точках поверхности, экспонированной в агрессивной среде.
Относительно слабая питтинговая коррозия, наблюдающаяся на нержавеющих сталях в процессе опреснения морской воды, содержащей сульфаты, по сравнению с ожидаемой, несомненно, связана с пассивирующими свойствами сульфат-ионов. В тех случаях, когда это возможно преднамеренное введение их также может дать большой эффект.
Питтинговой коррозии в водных растворах могут подвергаться Fe, Ni, Co, Al, Zr, Mg, нержавеющие стали, сплавы алюминия.
Если питтинговая коррозия проникает сквозь деформированный слой, то положительный эффект такой обработки теряется.
Происходила значительная питтинговая коррозия, причем, как показали исследования, некоторые питтинги достигали глубины почти 1 мм, несмотря на то, что система эксплуатировалась менее одного года. Было предположено, что причиной возникновения питтинговой коррозии является образование на трубах осадка окиси меди и использование неподходящего ингибитора.
| Коррозия малоуглеродистых сталей на разных глубинах в Атлантическом ( 1 – 4 и Тихом ( 5 – 7 океанах. |
Скорость питтинговой коррозии в аэрированной морской воде в стальных судовых трубопроводах может составлять до 1300 мкм / год. Питтинг может усиливаться, если на металле остается окалина. Как и в атмосферных условиях, окалина защищает только покрытую поверхность, а свободные участки становятся анодными. Ввиду сравнительно большой, как правило, площади катодных участков, скорость коррозии на локальных анодах очень велика.
История создания тефлона
Тефлон был впервые создан, как и многие чудодейственные химические вещества, в результате лабораторной аварии. В 1938 году Рой Дж. Планкетт, химик DuPont, экспериментировал с хладагентами, когда обнаружил белый воскообразный материал, который оказался очень скользким.
Это был инертный фторуглерод — политетрафторэтилен (ПТФЭ), который обладал превосходными антипригарными и водоотталкивающими свойствами. В 1945 году DuPont запатентовал химическое вещество под товарным знаком «Тефлон». Компания рекламировала его как «самый скользкий материал из существующих».

К 1948 году DuPont производил около 1.000 тонн тефлона ежегодно на своем заводе в Вашингтоне.
Для DuPont тефлон, который использовался для покрытия кастрюль и сковородок, оказался золотой жилой. Продажи тефлоновой посуды достигли пика 1.000.000.000 долларов в 2004 году.
Выбор контактирующих металлов
Между двумя различными соприкасающимися металлами (металлическими покрытиями) в присутствии влаги и загрязнений воздуха возникает гальваническая пара, начинается электролиз, в результате которого происходит быстрое разрушение более отрицательного металла (анода). Поэтому выбор контактируемых металлических поверхностей имеет большое значение.
При определении возможности применения ток или иной пары контактирующих металлов пользуются рядами нормальных потенциалов металлов. При этом часто нормальную разность потенциалов менее 0,5 в между двумя металлами принимают как допустимую. Такой подход является принципиально неправильным по следующим соображениям. а) Нормальные потенциалы определяются путем измерения потенциала металлов при 25° С по отношению к стандартному водородному электроду, который они имеют, когда ионная активность находится в состоянии равновесия с раствором своих собственных ионов. Корродирующие электроды, о которых в конечном итоге идет речь при рассмотрении комбинаций металлов по отношению к электролитам, естественно, нс находятся в состоянии равновесия.
б) Разности потенциалов не способствуют полному выявлению картины поведения в отношении коррозии, так как решающее влияние имеет кинетическое торможение. Elze и Oelsner предлагают некоторые практические ряды напряжений в конденсате (воде) н морской воде.
В качестве конденсата служит насыщенный воздухом буферный раствор фталата со значением рН-6 при 25° С и атмосферном давлении, а в качестве морской воды — искусственная морская вода со значением pH-7,5 при 25° С и атмосферном давлении. Значения электродных потенциалов в указанных электролитах приведены в табл. 12-7. По данным табл. 12-7 в нормальном ряду напряжений кадмий более благороден, чем железо, тогда как сталь в практических рядах напряжений металлов в конденсате и морской воде благороднее кадмия. Алюминий в указанных трех рядах напряжений имеет очень разные значения потенциалов.
Таблица 12-7
Электродные потенциалы некоторых металлов в различных рядах напряжений 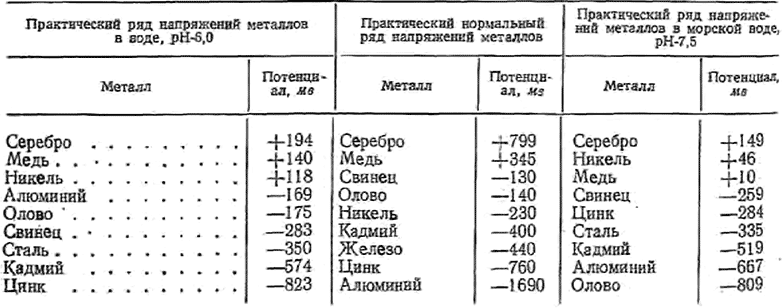
Между медью и никелем разность нормальных потенциалов составляет почти 600 мв, тогда как в практических рядах электродные потенциалы их близки.
В табл. 12-8 приведены данные о допустимых парах металлов для тропических и морских тропических условий, принятые для отечественного электрооборудования. При необходимости соприкосновения недопустимых таблицей пар следует или применять промежуточные покрытия для контакта, или разделять соприкасающиеся поверхности слоем лака, прокладками из пластмасс или других электроизоляционных материалов (пленки из фторопласта, лавсана, полиэтилена и др,). Полихлорвиниловые пленки применять не следует, так как при старении они выделяют соляную кислоту, что усиливает коррозию. Существенно замедляет контактную коррозию плотное сжатие деталей, которое препятствует проникновению между ними влаги. Контактная коррозия не наблюдалась, например, во влажной среде при плотных болтовых соединениях небольших деталей, даже если эти детали были изготовлены из материалов, не рекомендуемых табл. 12-8 для контакта, поскольку между такими деталями не проходил влажный воздух.
Замедлить процесс коррозии можно, применяя окраску контактирующих поверхностей надежными лакокрасочными покрытиями или смазку соприкасающихся металлических поверхностей. При пользовании электрохимическими рядами следует при оценке опасности контактной коррозии учитывать размеры деталей. Если соприкасаются маленькая и большая детали, то маленькая может сильно разрушаться, если потенциал ее будет в предполагаемой коррозионной среде более отрицательным, чем потенциал большой (т. е. если она будет анодом). Наоборот, если маленькая деталь является катодом, а большая — анодом, то существенного разрушения ни одной из этих деталей может не произойти.
Условия возникновения и распространения точечной коррозии
На распространение питтинга влияют:
- Концентрация и природа ионов, присутствующих в растворе;
- Характер катодного процесса.
Визуально вы можете видеть области без точек (катодные области), которые питают анодные реакции питтинга в процессе развития. После образования питтинг развивается с автостимолантным эффектом. Процесс аккреции может придать питтингу разные и непредсказуемые морфологические аспекты. Точечная коррозия может следовать направлению силы тяжести с вертикальным ростом или иметь тенденцию избегать механически очень устойчивых поверхностей (закаленных).
После появления точечной коррозии скорость коррозии достигает очень высоких значений, что приводит к ухудшению качества изделия за короткое время. Может случиться, что питтинг не продолжит свое проникающее действие: в случае, если нет необходимых условий для его роста, не образуется питтинг большей активности, который будет поглощать весь ток, подаваемый из области, окружающей катод. На скорость развития точечной коррозии очень сильно влияет восстановление ионов металлов по отношению к воздействию кислорода, которое ограничено растворимостью в растворе и диффузионными параметрами.
В основном, на процесс точечной коррозии очень влияют:
- Температура;
- Концентрация специфических ионов (Cl-) – чем выше концентрация этих ионов, тем интенсивность точечной коррозии становится более выраженной. Насыщенные растворы хлора определяют уменьшение процесса точечной коррозии, поскольку триггерные точки быстро размножаются, а затем коррозия приобретает общий вид с низкой скоростью проникновения. В этих условиях процесс точечной коррозии также останавливается после снижения растворимости кислорода, что недостаточно стимулирует анодное действие хлоридов, которые в этой ситуации имеют очень высокие скорости. Морская вода с процентным содержанием соли, равным 3%, представляет собой оптимальные условия для коррозии;
- рН раствор;
- Продукты коррозии – они нерастворимы и могут вызывать другие процессы локальной коррозии (щелевая коррозия);
- Наличие ионов кислорода – их присутствие препятствует точечной коррозии;
- Заусенцы, шероховатость поверхности, геометрические факторы;
- Металлографические факторы – мартенситные и ферритные структуры более благоприятны для точечной коррозии, чем аустенитные структуры, которые содержат в себе такие вещества, как молибден, хром, никель, которые снижают подверженность коррозии.
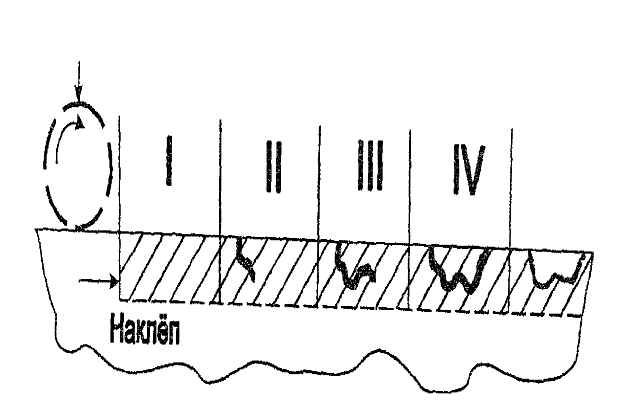
Процесс распространения обусловлен созданием гальванической пары, представленной на рисунке ниже.
Учитывая активно-пассивное поведение металла в растворе хлорида натрия (NaCl, морская вода), катодная реакция протекает по всей поверхности металла с образованием ионов ОН-, которые образуют больше катодных поверхностей вне питтинга. Анодная реакция растворения металла происходит внутри точки с образованием ионов металла и развитием диффузионных явлений, которые приводят к постепенному обогащению ионов хлора. Действие ионов хлоридов и повышение кислотности (развитие ионов Н+) обеспечивают состояние активности металла внутри полости; одновременно, образование продуктов коррозии, которые благодаря их более высокому удельному весу способствуют процессу коррозии в вертикальном направлении, увеличивая проникающую способность процесса.
Обеспечим защиту от питтинговой коррозии
Наша компания занимается профессиональным горячим цинкованием разных типов металлоконструкций. Мы предлагаем свои услуги с 2007 года. Есть сразу несколько причин обратиться к нам.
К ним относятся такие, как:
- Обширные производственные площади. Есть три цеха для горячего цинкования. Мощность производства – до 120 тонн в год.
- Универсальность. Мы работаем с разными категориями изделий. На предприятии установлена самая глубокая в ЦФО ванна для цинкования. Ее глубина составляет 3,43 метра.
- Гарантия качества. Весь процесс контролируется на соответствие с ГОСТ 9.307-89.
На предприятии используется современное оборудование от KVK KOERNER и EKOMOR. Работаем с разными категориями клиентов, готовы выполнить даже срочные заказы с минимальными затратами времени.
Чтобы рассчитать стоимость и оформить заказ, звоните по телефону или оставьте заявку на сайте.
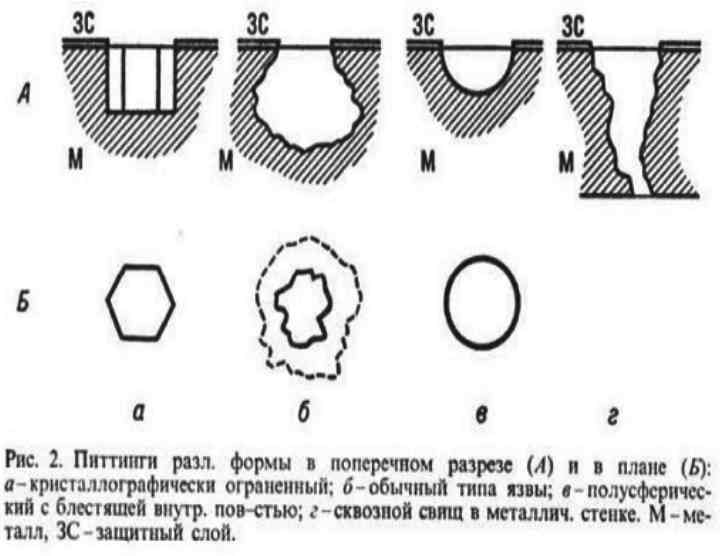
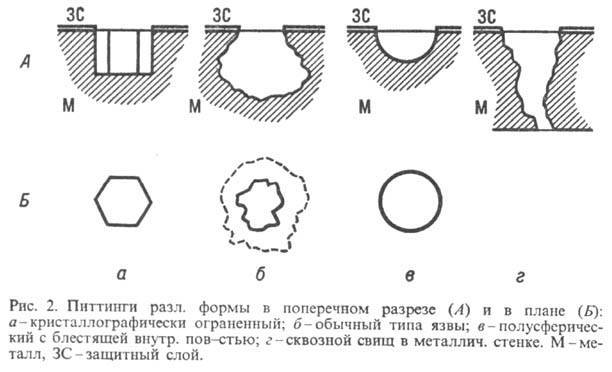
Виды питтинговой коррозии
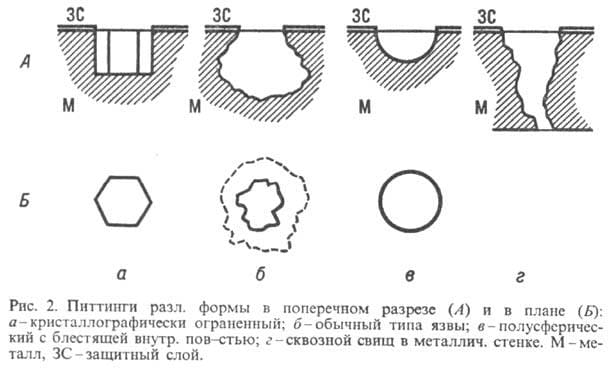
Среди параметров классификации питтинговой коррозии металла – тип питтинга, который появляется на поверхности металла:
- Поверхностный. Это один из наименее опасных вариантов ржавения. Он затрагивает только верхний слой металла. Со стороны можно опознать такое разрушение по появлению небольших линий, диаметр которых составляет до 3 мм. Чаще всего проблема наблюдается в угловых местах, а распространение начинается далее по изделию. Если среда благоприятная, то повреждение быстро затронет весь металл.
- Острый. Если в первом случае можно видеть линии, то здесь возникают большие точки, диаметр которых будет от 2 до 5 мм. Сначала появляется несколько точек, потом их становится больше. Некоторые соединяются и становятся намного больше. Таким образом металл в короткие сроки потеряет прочность.
- Закрытый. Такой питтинг находится изнутри металлической пленки. Здесь соединяются линии и точки. При этом сами размеры намного больше – от 5 до 15 мм. Это не самый распространенный вариант повреждения. До того момента, когда возникнет такой вариант коррозии, должно пройти намного больше времени. Одна из угроз в такой ситуации – процесс повреждения будет сложно остановить при помощи ингибиторов и других средств.
Необходимо обратить внимание на то, какой тип коррозии появился на металле, какая площадь была затронута. В такой случае можно будет понять, как решить проблему возникновения повреждений
9.Явление питтинга, как дефекта гальванических покрытий. Причины питтинга и способы его устранения.
Механизм
возникновения коррозионных ям —
питтинга, под воздействием кислорода
Питтинг
– микроскопические темные точки на
поверхности.
Питтинговая
(точечная) коррозия – вид коррозионного
разрушения, которому подвергаются
исключительно пассивные металлы и
сплавы. Питтинговая коррозия наблюдается
у никелевых, циркониевых, хромоникелевых,
хромистых, алюминиевых сплавах и др.
При
питтинговой (точечной) коррозии разрушению
подвергаются только отдельные участки
поверхности, на которых образуются
глубокие поражения – питтинги (точечные
язвы). Наблюдается питтинговая коррозия
при воздействии на металл или сплав не
только пассиваторов (приводят поверхность
в пассивное состояние, например,
окислитель), но и ионов-активаторов
(Cl-, Br-, J-). Активно протекает питтинговая
(точечная) коррозия в морской воде, смеси
азотной и соляной кислот, растворах
хлорного железа, других агрессивных
средах.
По
размерам питтинги различают:
–
микропиттинги (до 0,1 мм);
–
питтинги (0,1 – 1мм);
–
пятно, язва (более 1 мм).
Питтинг
может быть закрытым, открытым и
поверхностным.
Открытые
питтинги хорошо видны на поверхности
невооруженным глазом или под небольшим
увеличением. Если открытых питтингов
очень много – коррозия приобретает
сплошной характер. В открытом питтинге
дно поры выступает в качестве анода, а
пассивная пленка – катода.
Закрытые
питтинги – очень опасный вид коррозионного
разрушения, т.к., такие повреждения
нельзя увидеть воочию, определить их
наличие можно лишь по специальным
приборам. Закрытые питтинги развиваются
вглубь металла или сплава. Закрытый
питтинг может послужить причиной пробоя
даже в нержавеющих сталях.
Поверхностный
питтинг – вид питтинга, который
развивается больше вширь, чем вглубь,
образуя на поверхности металла или
сплава выбоины.
Этапы
роста питтинга:
1)
Зарождение питтинга происходит в местах
дефектов пассивной пленки (царапины,
разрывы) или ее слабых местах (если
имеет место неоднородность сплава) при
достижении определенного потенциала
– потенциала питтингообразования (φпо).
Ионы-активаторы вытесняют адсорбированный
на поверхности кислород или при
взаимодействии разрушают оксидную
защитную пленку.
2)
Рост питтинга – происходит по
электрохимическому механизму, вследствии
интенсивного растворения пассивной
оксидной пленки. Из-за активного
растворения пленки происходит усиление
анодного процесса в самом питтинге
(активационный рост питтинга). Со
временем, когда питтинг будет достаточно
расширен, активационный рост замедляется,
начинается диффузионный режим роста
питтинга.
3)
Иногда рост питтинга прекращается и
наступает стадия репассивации. Основной
причиной репассивации можно считать
сдвиг потенциала поверхности в
отрицательную сторону, т.е. сторону
пассивации. Питтинг с диффузионным
режимом роста (постепенно, стабильно
растущий питтинг) не может перейти в
стадию репассивации.
Склонность
к питтинговой коррозии определяется
некоторыми факторами:
–
природой металла или сплава (склоны к
образованию питтингов алюминий, никель,
цинк; молибден, хром, кремний и др.
питтингообразованию не подвергаются);
–
температурой (с повышением температуры
растет количество питтингов);
–
состоянием поверхности (хорошо
отполированная поверхность более
стойкая, чем шероховатая);
– рН
среды (чаще возникают питтинги в кислых
средах);
–
примесями в среде (наличием
ионов-активаторов).
Защита
металлов и сплавов от питтинговой
(точечной) коррозии осуществляется
следующими методами:
1)
Электрохимическая катодная и анодная
защита (иногда вместе с ингибиторами);
2)
Подбор специальных материалов, которые
не подвергаются питтинговой (точечной)
коррозии. Повышению стойкости способствуют
введение в состав сплава хрома, молибдена,
кремния и др. стойких металлов.
3)
Ингибирование замкнутых систем
(применение нитратов, щелочей, хроматов,
сульфатов)
4)
добавление антипиттинговых добавок,
улучшающих смачивание электролиза.
5)Идеальная
защита от коррозии на 80% обеспечивается
правильной подготовкой поверхности, и
только на 20% качеством используемых
лакокрасочных материалов и способом
их нанесения.
Подготовка
поверхности заключается в предварительной
подготовке, имеющей целью устранение
окалины, ржавчины и посторонних веществ,
если они имеются, со стальной поверхности
перед нанесением заводской грунтовки.
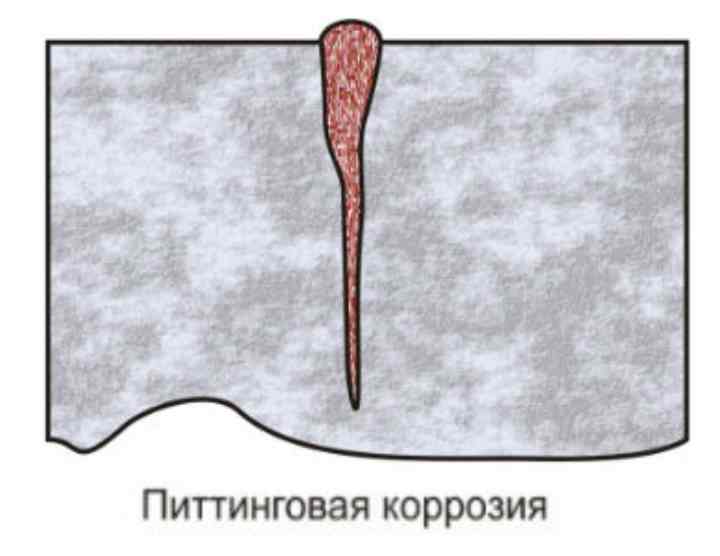
Что такое питтинги или питтинговая коррозия
Разрушение верхней оболочки металлических материалов из-за воздействия воды или кислоты называется коррозией.
Из-за разрешения внешних слоев материал теряет свою прочность, эластичность и электропроводность. Свойства металлического изделия ухудшается.
При частой эксплуатации изделий из металла со времени они разрушаются под воздействием определенных факторов. К наиболее опасным типам коррозии относят питтинговую.
Чтобы выяснить как защитить металл от ржавчины, и надолго сохранить его свойства. Следует выяснить, что из себя представляют питтинги, и как они образуются на разных поверхностях.
Классификация коррозии в зависимости от типа окружающей среды
Атмосферная коррозия
Это один из самых распространенных видов коррозии, который в зависимости от объема влаги, воздействующей на металлическую поверхность, также классифицируется как мокрая, сухая и влажная коррозия. При этом в зависимости от агрессивности атмосферы выделяют следующие виды атмосферной коррозии, которая может проявляться:
- в промышленности;
- сельской местности;
- приморских районах;
- при специфическом загрязнении окружающей среды.
Главные особенности атмосферной коррозии проявляются в скорости ее распространения. На этот фактор оказывают влияние такие параметры, как температура, уровень влажности, состав металла, качество его поверхности, особенности состава окружающей среды, а также другие параметры.
Почвенная коррозия
Коррозийные процессы, проходящие с металлами в грунте или под землей, оказывают на их эксплуатационные характеристики разрушительное воздействие. Существует не только почвенная коррозия металлов, но также процесс, который возникает после воздействия внешних и блуждающих электротоков.
Под напряжением коррозийные процессы протекают вследствие одновременного воздействия на поверхность металлоконструкций коррозийной среды и механических напряжений. Как следствие, на поверхности металлоконструкции может наблюдаться коррозийное растрескивание или коррозийная усталость. Это зависит от вида и интенсивности напряжения.
Щелевая коррозия металла
Щелевая коррозия развивается вследствие контакта изделий в электропроводящих средах, имеющих разные электрохимические характеристики. Помимо этого различают коррозийные процессы в зависимости от разновидности и сложности вызываемых повреждений – это сплошная (или общая) и местная (или локальная) коррозия.
Между тем, сплошная коррозия может быть равномерной (процесс проходит с одинаковой скоростью по всей площади металлоконструкции) и неравномерной (на разных участках детали процесс протекает с разной скоростью).
Локальный коррозийный процесс классифицируют на сосредоточенный (проявляется в виде пятен, язв, точек и др.) и подповерхностный (транс- и межкристаллитный, структурно-избирательный).
Если же говорить об изделиях, поверхность которых обработана по технологии горячего цинкования, то в данном случае большую угрозу несет общая коррозия. Она вызывает разрушение защитного слоя, что приводит к утрате изделием первоначального привлекательного внешнего вида.
Также для продукции, имеющей цинковый слой, нанесенный горячим цинкованием, опасность несет коррозия под напряжением (разрушение происходит на наиболее напряженных участках детали) и точечная (питтинговая) коррозия (по аналогичным причинам).
Появление – питтинг
При анодном растворении титана и его сплавов с понижением плотности тока возрастает вероятность появления питтингов. При плотности тока выше 15 А / см2 этого не наблюдается.
Результаты испытаний в области критической концентрации хромата не очень хорошо воспроизводимы вследствие непостоянства появления питтинга.
| Зависимость степени увеличения скорости ( 3 ( РРа. |
Интенсивное растворение железа при замедленном переходе в раствор хрома и марганца в условиях воздействия растягивающих напряжений приводит к появлению питтингов, локальных коррозионных поражений, которые хорошо наблюдаются визуально. Наблюдения показали также, что питтинги являются местом зарождения трещин.
Помимо перечисленных факторов образование питтинга зависит от твердости материала, нагрузки, степени обработки поверхности и др. С увеличением твердости материала время до появления питтинга возрастает.
Зачастую в аэрированной горячей воде при 60 С и выше происходит смена полярности находящихся в контакте цинка и железа ; при этом цинк приобретает свойства, характерные для коррозионностойкого, а не протекторного покрытия; следовательно, в этом случае цинковое покрытие способствует появлению питтингов на стали.
| Влияние концентрации Rh ( / и Н, SO4 ( 2 на выход металла по току.| Влияние температуры и перемешивания ( /, 2 на выход Rh по току в электролите, содержащем ( г / л 6Rh. ( SO4 ( в пересчете на металл, 52 8 мл / л H SO4, 4 5 ( N Н4 а SO4, при плотности тока ( А / дм. / – 0 6. 2, 3 – 1 25. 4 – 2 5. |
Электролит № 1 применяют для осаждения покрытий толщиной 3 мкм, электролиты № 2, 3 – для получения осадков 3 мкм. Во избежание появления питтинга осаждение покрытий из указанных электролитов рекомендуется производить при движении катодной штанги.
График функции / ( х) показывает, что участки, прилегающие к вершине, хорошо защищаются катодным током, тогда как устье трещины не испытывает заметного действия анода вершины. Поскольку при появлении питтинга в начальный период образования трещины неповрежденная поверхность металла пришла в относительно катодное состояние, то стенки в устье трещины становятся относительно анодными и ускоряется коррозионное растворение металла, расширяющее устье.
Причины возникновения данного явления полностью до сих пор не выяснены. Однако установлено, что на появление питтинга влияет наличие в электролите железа, органических загрязнений и взвешенных частиц. Мнение о том, что с увеличением концентрации водородных ионов в электролите образование питтпнга усиливается, не подтвердилось. Ряд исследовании показал, что при низких значениях рН на покрываемой поверхности образуются многочисленные мелкие пузырьки водорода, которые, однако, быстро удаляются. В электро литах с большим значением рН образуется меньшее количество пузырьков водорода, но больших размеров, причем пузырьки дольше остаются на катодной поверхности и могут достичь значительной величины.
Фреттинг-коррозия возникает вследствие малых вибрационных смещений контактных поверхностей друг относительно друга, если одна из них или обе металлические. Обычно коррозия этого типа сопровождается появлением питтингов на контактирующих поверхностях. Оксиды и продукты истирания металла заполняют питтинги, так что они становятся заметны только после удаления этих продуктов.
Существует несколько теорий питтингобразования. В частности, считается, что появление питтинга связано с привариванием материала одного трущегося тела к другому или с интенсивным окислением и пластической деформацией в поверхностных слоях металла, а также с повторяющимися деформациями волочения и смятия, что в конечном счете приводит к усталости металла.
Наоборот, краевой угол пузырька будет иметь наибольшую величину в том случае, если заряд поверхности равен нулю. Следовательно, можно сделать заключение, что появление питтинга на никелевом катоде наиболее вероятно, когда потенциал катода близок к потенциалу нулевого заряда. При этом пузырьки будут обладать наибольшими размерами.
Он начинается с непрерывного роста тока и появления первых питтингов микрометрового размера. Нарастание концентрации Fe2 со временем является хорошим индикатором наличия питтингов.
Загрязнение железом приводит к росту внутренних напряжений в покрытии, следствием чего является хрупкость никеля. Коллоидальная взвесь соединений железа, появляющаяся в никелевой ванне, может служить причиной появления сильного питтинга.
Как защитить металл
Мы рассмотрели вопрос о том, из-за чего возникает питтинговая коррозия. При понимании особенности такого процесса, можно будет определить, как с ней бороться и обеспечить процесс защиты.
Чтобы бороться с такой проблемой, можно будет использовать процесс пассивации.
Он основан на применении специального раствора, в состав которого входят две кислоты – лимонная и азотная. Также для сильного усиления процесса, можно использовать добавки.
Цель, которая ставится при применении пассивации, процесс коррозии может стать медленнее или же прекратиться.
Есть 3 метода, позволяющие защититься от причин возникновения питтинговой коррозии.
К ним относятся:
- Устранение дефектов. Использование современных методов позволяет устранить большинство видов дефектов, которые могут появляться на металле. Применяется полировка, а также другие средства для исправления неровностей. Это уменьшает опасность развития коррозии.
- Полировка. Помогает устранить шероховатости. Это не позволяет продуктам коррозии скапливаться. На гладком металле могут появиться естественные защитные пленки.
- Использование хромированного покрытия. Оно позволяет оградить материал от контакта с агрессивными средами. Используется цинкование – именно такой подход помогает улучшить общее качество защиты.
Наша компания всегда готова создать защиту от повреждений любых видов металлоконструкций и стальных изделий.